RESEARCH
General Research Profile
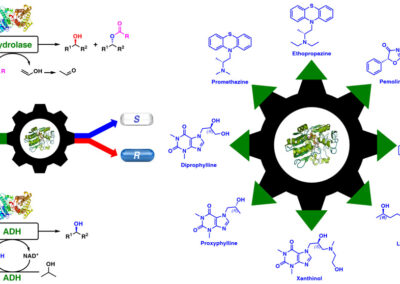
Our research interests mostly aim at creating new chemoenzymatic strategies toward active pharmaceutical ingredients (APIs) as well as novel therapeutic complex molecules potentially useful in the treatment of various life-threatening diseases. In this regard, we strive to find efficient crossroads and synergies between Biocatalysis and Medicinal Chemistry for developing future Industrial Biotechnology and Sustainable Bioeconomy.
We focus our particular attention at application of hydrolytic enzymes (in particular lipases) in kinetic resolutions of racemic alcohols or esters, but more recently, thanks to co-operation with Prof. Wolfgang Kroutil from The University of Graz, we also extended our research towards stereoselective biocatalytic (hydrogen transfer) reductions of prochiral ketones and keto-esters catalyzed by recombinant alcohol dehydrogenases (ADHs) and/or wild-type microbial whole cells. We have also long-term experience in designing and synthesis of novel clinically-important small molecules potentially useful in prevention of infectious diseases as well as optimization and scale-up of enzymatic processes to pre-industrial commercial batch size.
In addition, one of our favorite research topics is computational biology, which helps us to provide a deeper understanding of the mechanisms and molecular basis of catalytic behavior of enzymes that we use in vitro in our daily routine. We are also fascinated by nature’s biodiversity in terms of natural products biosynthesis and keeping in mind all the treasuries tricks that ‘mother Nature’ inspires us we try to ‘design and produce’ our own synthetic molecules.
Detailed Research Field
Our research portfolio encompasses several scientific activities that are focused on:
CHEMOENZYMATIC SYNTHESIS
- The use of enzymes and/or whole-cell microorganisms as biocatalysts for the efficient synthesis of useful compounds, especially enantiomeric pharmaceuticals and/or pharmacologically relevant agents;
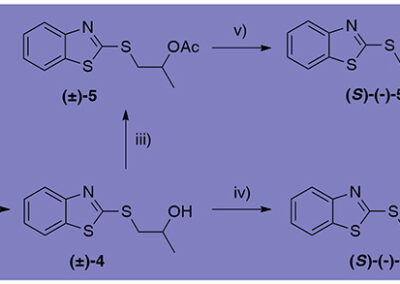
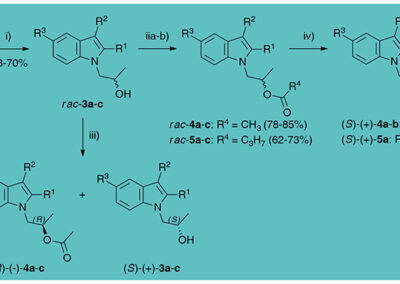
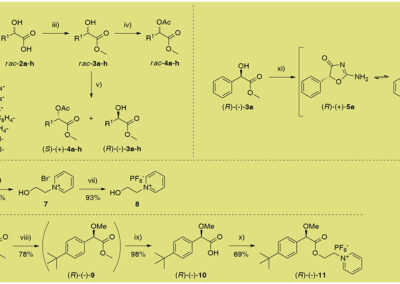
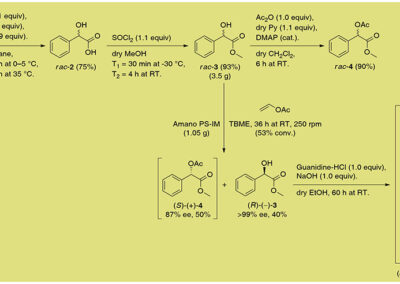
- Development of lipase-catalyzed kinetic resolution (KR) of racemic alcohols/esters;
- Synthesis of chiral alcohols by asymmetric hydrogen-transfer bioreduction employing recombinant alcohol dehydrogenases (ADHs);
- Expanding substrate scope for lipases and oxidoreductases;
- Application of immobilized enzymes in chemical synthesis;
- Application of whole-cell system in chemical synthesis;
- Invention of novel reagents (acyl donors) for efficient, chromatography-free lipase-catalyzed KR approaches towards sec-alcohols;
- Studies on one-pot/two-step deracemization procedures for sec-alcohols via a tandem bi-enzymatic oxidation–reduction reaction sequence based on (laccase/TEMPO)-ketoreductase (KRED) catalytic systems;
- Intensification of enzymatic processes using chemical and physicochemical methods;
- Screening of biocatalysts in terms of their application in organic synthesis;
- Optimization and scale-up of enzymatic processes.
MEDICINAL CHEMISTRY
- Synthesis of innovative and/or generic pharmaceuticals;
- Design and synthesis of potential inhibitors of protein kinase CK2;
- Design and synthesis of new anticancer and antifungal agents;
- Development of new hybrid molecules possessing dual anti-cancer/anti-fungal activity;
- Synthesis of libraries of biologically active compounds possessing antimicrobial activity.
ANALYTICAL CHEMISTRY
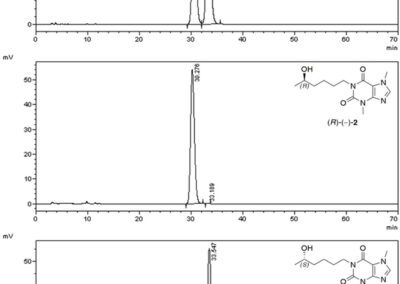
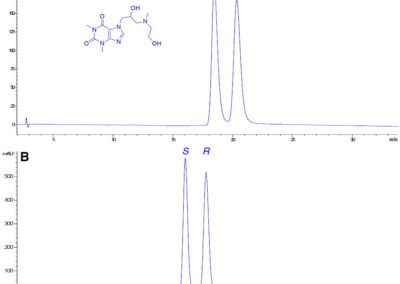
- Development of analytical methods for the detection/monitoring of enzymatic reactions progress (GC, HPLC);
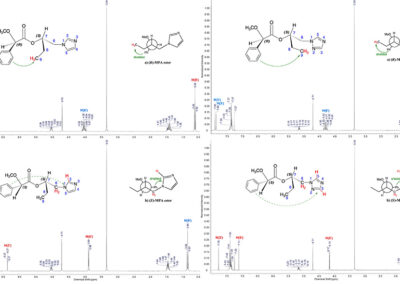
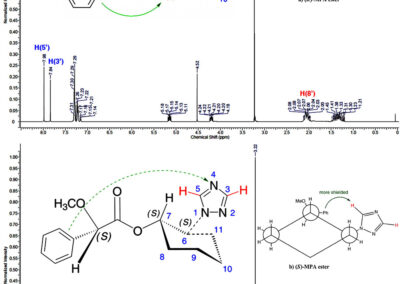
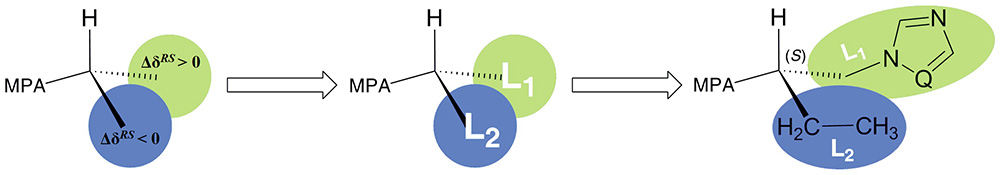
- Assignment of the absolute configuration of novel liquid and/or non–crystalline optically active compounds using spectroscopic methods employing chiral derivatizing agents (CDAs);
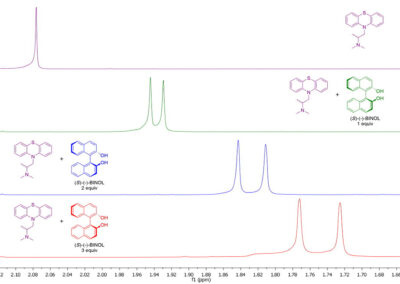
- Determination of the enantiomeric purity of optically active compounds employing chiral HPLC and/or NMR spectroscopy using chiral solvating agents (CSAs).
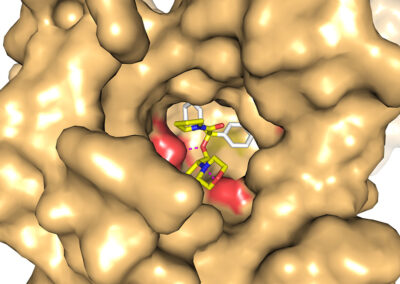
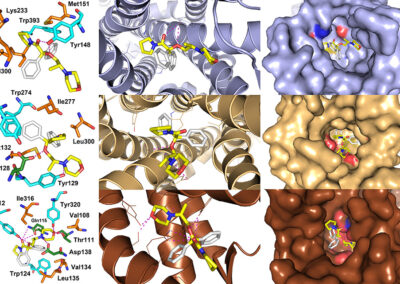
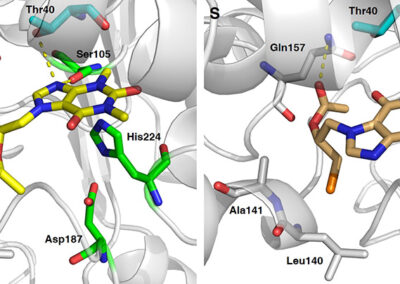
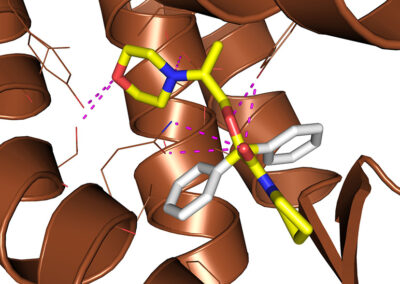
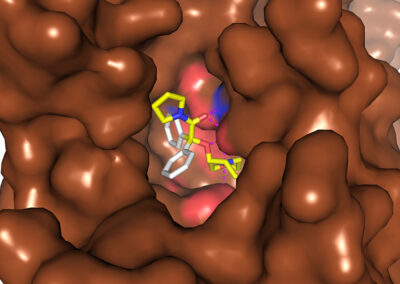
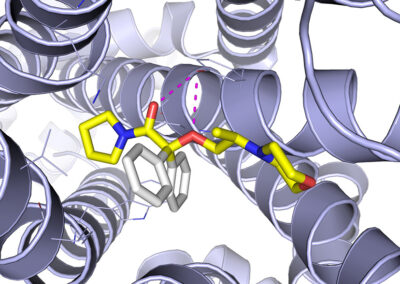
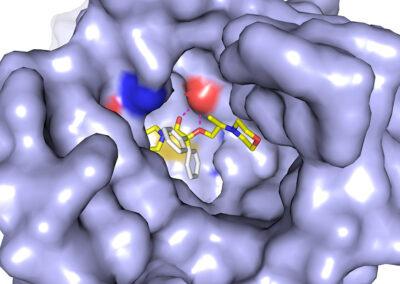
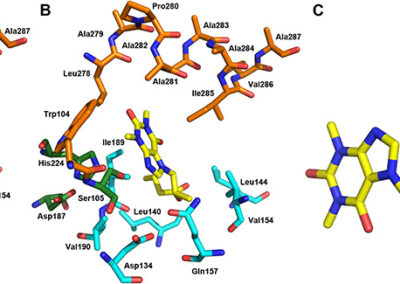
IN SILICO CALCULATIONS
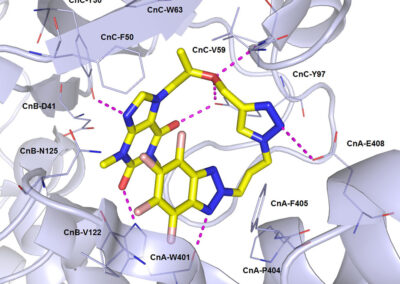
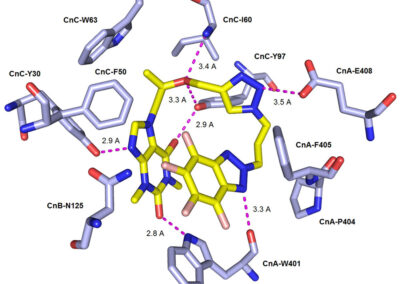
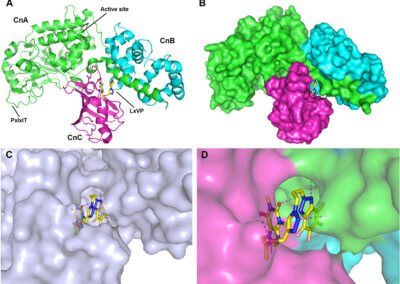
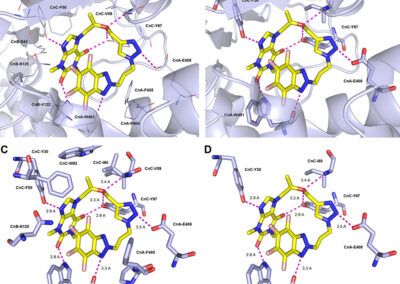
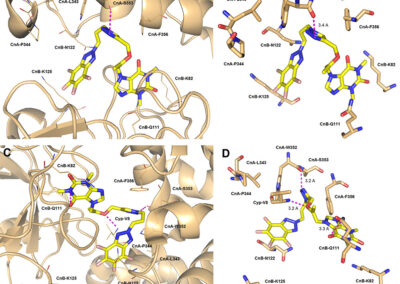
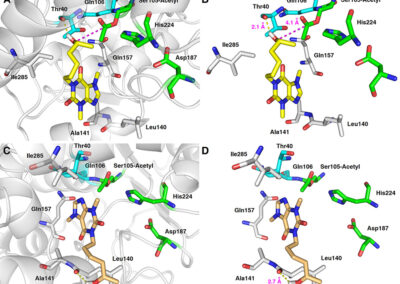
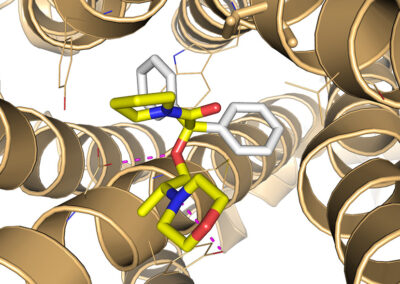
- Ligand docking simulations using Autodock Vina and/or GOLD© CCDC software;
- In silico studies of ligand-receptor interactions;
- Computer-aided structure-based design for modeling new inhibitors of target proteins (kinases, calcineurin, opioid receptors etc.);
- Structure-activity relationship (SAR) of the newly synthesized biologically active agents;
- Prediction and rationalization of stereoselectivity (stereopreference) of enzymes as biocatalysts.
The social meaning of our research and the practical application of its results
The development of new pharmaceuticals can cost upward of a billion dollars and take over a decade before the drug reaches the market. Even brilliant new drug inventions intellectually protected by costly patent applications are ‘unconsumable’ by most of the pharmaceutical companies due to high investment’s risk of innovative APIs registration process. Therefore, instead of patenting inventions of novel potential medications, we present our research findings as a pro publico bono publications. Moreover, we strongly believe that providing innovative (safer, more efficient & selective) methods for the synthesis of enantiomeric drugs that are already FDA/EMA-approved is more supportive for generic APIs manufacturing and will allow smaller pharmaceutical companies to increase their competitiveness against the global pharma tycoons. Some may accuse us of being ‘useful idiots’, but that is why we chose the academic pathway, so that the science we do … serves not only large corporations!
Potential areas of collaboration
We are especially interested in novel enzymes for which little catalytical information is available, so that we could help to answer vital questions about the activity and function of these proteins. For potential industrial partners we offer our lab skills and ‘know-how’ in development of alternative chemoenzymatic routes toward enantiomeric APIs.
EQUIPMENT
We are fortunate to harbour up-to-date chemical and analytical equipment that play a pivotal role in enabling our aims and objectives. Among the analytical instrumentations are, i.e. gas chromatographs (two Agilent GCs and one ‘oldie’ HP), high-performance liquid chromatographs (two Shimadzu HPLCs adopted for normal-phase mode analyses and one ‘oldie’ Perkin Elmer apparatus adopted for reversed-phase analyses) and single polarimeter (Atago AP-300). Other small (general use) equipment, including analytical balances (1 × Ohaus and 2 × Radwag); magnetic stirrers (IKA and Heidolph), laboratory shakers (Heidolph); glass and/or steel pressure reactors (Pressure Vessels-Ace Glass); laboratory centrifuges; rotary evaporators (Büchi and Heidolph); oil and diaphragm pumps; Kugelrohr bulb-to-bulb apparatus; UV lamps; home-made photoreactors for UV and visible light irradiation; point apparatus; ultrasonic cleaners, pH-meters are within reach.
Scope of Research (For polish speakers):
Opis tematyki badawczej.
Zespół specjalizuje się w prowadzeniu badań:
- nad opracowaniem wydajnych chemoenzymatycznych syntez aktywnych składników farmaceutycznych (API) i/lub ich optycznie czynnych prekursorów;
- nad możliwością zastosowania biokatalizy w asymetrycznej syntezie optycznie czynnych związków o znaczeniu biologicznym, ze szczególnym uwzględnieniem pochodnych o udokumentowanej aktywności przeciwnowotworowej, przeciwdrobnoustrojowej oraz biocydowej;
- z zakresu chemii leków innowacyjnych, skupionych na różnych aspektach komputerowego projektowania oraz syntezy nowych związków o potencjalnej aktywności przeciwnowotworowej (gł. z grupy inhibitorów ludzkiej kinazy białkowej CK2) oraz przeciwgrzybowej (inhibitory kalcyneuryny);
- nad opracowywaniem procedur rozdziałów kinetycznych (KR) mieszanin racemicznych alkoholi II-rzędowych i/lub odpowiednich estrów z zastosowaniem lipaz jako biokatalizatorów;
- nad opracowywaniem procedur stereoselektywnej redukcji prochiralnych związków karbonylowych z zastosowaniem mikroorganizmów i/lub rekombinowanych dehydrogenaz alkoholowych;
- nad syntezą nowych odczynników dedykowanych reakcjom katalizowanym lipazami celem uzyskania poprawy efektywności rozdziałów kinetycznych oraz uproszczenia procesów wydzielania produktów bez konieczności stosowania technik chromatograficznych;
- nad powiększaniem skali procesów chemoenzymatycznych (biotechnologicznych);
- nad racjonalizacją wyników eksperymentalnych z użyciem dokowania molekularnego (wyznaczanie stereopreferencji enzymów w procesach katalitycznych; analiza oddziaływań białko-ligand);
- nad opracowaniem metod analitycznych do detekcji/monitoringu procesów enzymatycznych oraz do oznaczania czystości chemicznej i enancjomerycznej otrzymywanych produktów (chromatografia gazowa, chiralne HPLC, spektroskopia NMR);
- nad określaniem budowy przestrzennej nowych nieracemicznych związków organicznych przy użyciu metod spektroskopowych z zastosowaniem chiralnych odczynników derywatyzujących (CDAs) oraz chiralnych odczynników solwatujących (CSAs).
Potencjalne płaszczyzny współpracy.
- Projektowanie alternatywnych metod syntezy optycznie czynnych składników czynnych leków z zastosowaniem metod biokatalitycznych oraz klasycznej syntezy organicznej;
- Selekcjonowanie odpowiednich biokatalizatorów pod kątem ich zastosowania w syntezie organicznej;
- Poszukiwanie nowych rekombinowanych enzymów o dużym potencjalnie biotechnologicznym;
- Optymalizacja warunków procesów biotransformacji wybranych związków organicznych;
- Intensyfikacja procesów enzymatycznych z użyciem metod chemicznych oraz fizykochemicznych;
- Opracowywanie warunków analiz GC oraz HPLC;
- Oczyszczanie oraz charakterystyka spektralna i chiralooptyczna stereoizomerów;
- Synteza bibliotek związków do badań biologicznych;
- Publikowanie oraz patentowanie innowacyjnych rozwiązań chemicznych i/lub biotechnologicznych;
- Przygotowywanie wspólnych wniosków projektowych oraz aplikowanie o granty konsorcyjne w krajowych agendach naukowych (NCBiR).
Oferta dedykowana jest dla firm sektora: farmaceutycznego, biotechnologicznego oraz chemicznego.
Społeczny sens prowadzonych badań oraz praktyczne zastosowania efektów pracy.
Nasze dokonania w zakresie katalizy enzymatycznej oraz chemii medycznej przyczyniają się na co dzień do poszerzania puli chiralnych związków użytecznych w przemyśle chemicznym i farmaceutycznym. Badania prowadzone przez naszą grupę propagują stosowanie innowacyjnych oraz przyjaznych środowisku biotechnologicznych procedur syntezy, doskonale wpisując się przy tym w nowoczesne trendy światowej gospodarki. Wyniki naszych badań stanowią potencjalne wsparcie dla rodzimego przemysłu farmaceutycznego, będąc przydatnym źródłem wiedzy dla opracowań nowych leków w takich obszarach terapeutycznych jak: choroby onkologiczne, choroby zakaźne, choroby układu kostnego, a także choroby układu nerwowego oraz oddechowego. Ponadto, opracowane przeze naszą grupę syntezy kilku farmakologicznie czynnych związków o właściwościach przeciwnowotworowych oraz przeciwdrobnoustrojowych, a także czynnych farmaceutycznie składników leków (m. in. prometazyny, profenaminy, proksyfiliny, diprofiliny, nikotynianu ksantynolu, pemoliny i in.) mogą dzięki niskim kosztom wytwarzania, znakomitej czystości chemicznej oraz enancjomerycznej, czy też przyjaznym dla środowiska procesom chemoenzymatycznym, nie tylko poszerzyć portfolio krajowych przedsiębiorstw farmaceutycznych, ale również pozwolić zwiększyć ich konkurencyjność przy produkcji leków generycznych zarówno na rynku polskim jak i ogólnoświatowym. Na co dzień jesteśmy gotowi wspierać rodzimy przemysł farmaceutyczny i biotechnologiczny swoją wiedzą i doświadczeniem z zakresy otrzymywania enancjomerycznych API z wykorzystaniem enzymów na kluczowych etapach syntez (vide w rozdziałach mieszanin racemicznych, ‘chiralnym doczyszczaniu’ enancjomerów, stereoselektywnych bioredukcjach etc.) oraz analizy chiralnych produktów (oznaczenia: HPLC, GC, NMR, polarymetryczne).
Aparatura analityczna.
- Chromatografy gazowe (3 aparaty GC; Agilent & HP);
- Wysokosprawne chromatografy cieczowe (3 aparaty HPLC; Shimadzu & Perkin-Elmer);
- Kolumny analityczne do HPLC z chiralną fazą stacjonarną (Daicel & Phenomenex).
- Polarymetr (Atago AP-300);
- Wagi analityczne (1 × Ohaus oraz 2 × Radwag);
Aparatura chemiczna.
- Mieszadła magnetyczne i wytrząsarki laboratoryjne;
- Szklane oraz stalowe reaktory ciśnieniowe;
- Wirówki laboratoryjne;
- Wyparki obrotowe;
- Pompy olejowe i membranowe;
- Aparat do destylacji krótko-drożnej (ang. ‘bulb-to-bulb’) typu Kugelrohr;
- Lampy UV (254 nm oraz 336 nm);
- Fotoreaktory do naświetlania reakcji chemicznych światłem UV oraz widzialnym;
- Aparaty do pomiaru temperatury topnienia;
- pH-metry;
- Płuczki ultradźwiękowe etc.